Cykloheksan
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C6H12 | ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa | 84,16 g/mol | ||||||||||||||||||||||||||||||||||||||||
| Wygląd | łatwopalna, przezroczysta, bezbarwna ciecz[1] | ||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 110-82-7 | ||||||||||||||||||||||||||||||||||||||||
| PubChem | 8078 | ||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03561 | ||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||
| Pochodne | |||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
Cykloheksan – organiczny związek chemiczny, nasycony węglowodór alicykliczny zawierający sześć atomów węgla.
Właściwości fizyczne
W temperaturze pokojowej jest to bezbarwna, łatwopalna ciecz, bardzo słabo rozpuszczająca się w wodzie. Cykloheksan jest rozpuszczalnikiem olejów, tłuszczów, wosków i żywic.
Wytwarzanie
Cykloheksan otrzymuje się w destylacji niektórych gatunków ropy naftowej. Syntetycznie można go uzyskać przez katalityczne uwodornienie benzenu.
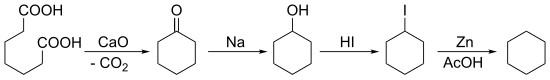
Znane są też dwie historyczne metody syntezy cykloheksanu. Pierwsza, opracowana przez Baeyera w 1894 roku, oparta jest na kondensacji Dieckmanna, w której substratem jest kwas pimelinowy:
Drugą metodę opracowali E. Haworth i W.H. Perkin jr. w tym samym roku i została oparta na reakcji Wurtza, w której substratem był 1,6-dibromoheksan:
Zastosowania
Cykloheksan jest popularnym rozpuszczalnikiem apolarnym. Znajduje zastosowanie w syntezie organicznej, w reakcjach, w których nie można stosować rozpuszczalników zawierających grupy metylowe. Jest też wykorzystywany jako rozpuszczalnik w szeregu spektroskopowych metod identyfikacji związków chemicznych.
Cykloheksan stosowany jest w syntezie poliamidowych włókien sztucznych.
Stereochemia
Czterowiązalne atomy węgla (w hybrydyzacji sp³) wymagają, by ich podstawniki tworzyły czworościan (hipoteza van't Hoffa i Le Bella)[a]. Pierścień sześciowęglowy spełniający takie wymagania musi być niepłaski. Możliwych jest pięć różnych ułożeń atomów węgla, przy których takie czworościenne otoczenie jest zachowane.
Najstabilniejszą, trwałą w temperaturze pokojowej konformacją pierścienia cykloheksanowego jest konformacja krzesłowa. W temperaturze pokojowej istnieje stan równowagi między dwoma konformacjami krzesłowymi, które są lustrzanymi odbiciami. W procesie przejścia jednego krzesła w drugie (tzw. inwersji pierścienia) stanami przejściowymi są pozostałe konformacje cykloheksanu (również niepłaskie): pół-krzesła, skręconej łódki, i łódki.
-
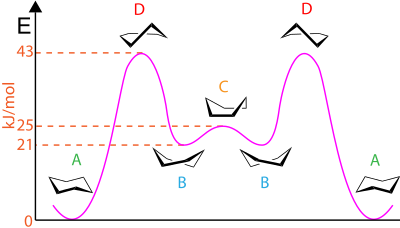 Konformacje pierścienia cykloheksanu w zależności od energii (oś pionowa), A – krzesło, B – skręcona łódka, C – łódka, D – pół-krzesło
Konformacje pierścienia cykloheksanu w zależności od energii (oś pionowa), A – krzesło, B – skręcona łódka, C – łódka, D – pół-krzesło
Wprowadzenie podstawników do pierścienia cykloheksanu może w znacznym stopniu zaburzyć geometrię pierścienia i szybkość przekształceń konformacyjnych.
Nierównocenność atomów wodoru w cykloheksanie
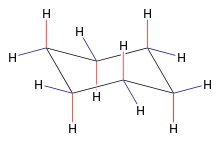
Atomy wodoru w cykloheksanie nie są równocenne. W cząsteczce tej można wyróżnić dwie grupy wodorów, różniące się istotnie właściwościami – tak reaktywnością, jak i właściwościami spektroskopowymi. Atomy aksjalne, połączone są ze szkieletem węglowym wiązaniami równoległymi do sześciokrotnej osi symetrii cząsteczki. Pozostałe nazywane są ekwatorialnymi.
Konsekwencją nierównocenności atomów wodoru w cykloheksanie jest izomeria geometryczna tzw. aksjalno-ekwatorialna jego pochodnych.
Uwagi
- ↑ Jest to równoznaczne z kątami pomiędzy wiązaniami R−C−R wynoszącymi 109,5°.
Przypisy
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4 .
- ↑ a b c d e Haynes 2016 ↓, s. 3-132.
- ↑ Haynes 2016 ↓, s. 5-174.
- ↑ a b c d Haynes 2016 ↓, s. 15-15.
- ↑ a b Haynes 2016 ↓, s. 5-145.
- ↑ a b c Haynes 2016 ↓, s. 6-69.
- ↑ Haynes 2016 ↓, s. 6-244.
- ↑ Haynes 2016 ↓, s. 6-191.
- ↑ a b c Cyclohexane, karta charakterystyki produktu Sigma-Aldrich, Merck, 26 lipca 2021, numer katalogowy: 650455 [dostęp 2022-06-24] . (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b Cyclohexane, [w:] ChemIDplus, United States National Library of Medicine [dostęp 2022-06-24] (ang.).
- ↑ Cyclohexane, [w:] CAMEO Chemicals, National Oceanic and Atmospheric Administration [dostęp 2022-06-24] (ang.).
Bibliografia
- CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, ISBN 978-1-4987-5429-3 (ang.).
- p
- d
- e
|
- Britannica: science/cyclohexane
- Universalis: cyclohexane
- БРЭ: 4677064
- SNL: sykloheksan
- DSDE: cyklohexan