Styren
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C8H8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | C | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 104,15 g/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwna, oleista ciecz[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 100-42-5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 7501 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Styren (winylobenzen) – organiczny związek chemiczny, węglowodór aromatyczny z alkenowym łańcuchem bocznym. Jest związkiem wyjściowym do produkcji polistyrenu[11].
Historia
W Polsce przed wybuchem II wojny światowej proces technologiczny otrzymywania styrenu opracował polski chemik Kazimierz Smoleński[12].
Otrzymywanie
Główną metodą otrzymywania styrenu jest dehydrogenacja etylobenzenu[11]:
Styren można także otrzymać poprzez eliminację chlorowodoru z chloroetylobenzenu[11] lub uwodornianie fenyloacetylenu przy użyciu katalizatora Lindlara(inne języki)[13]:
Właściwości
Styren w warunkach normalnych jest bezbarwną lub lekko żółtawą cieczą o słabym, charakterystycznym, nieprzyjemnym zapachu. Styren łatwo i szybko ulega polimeryzacji, nawet pod wpływem promieni słonecznych lub niezbyt intensywnego ogrzewania, tworząc polistyren:
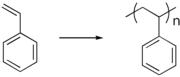
Łatwo polimeryzuje z butadienem, akrylonitrylem, estrami kwasów organicznych (np. akrylowego i metakrylowego), tworząc odpowiednie kopolimery i żywice polimerowe. Wchodzi w gwałtowne reakcje z silnymi utleniaczami.
Zastosowanie
Styren w dużych ilościach stosowany jest do otrzymywania polistyrenu, kopolimerów styrenowych, kauczuków syntetycznych oraz żywic butadienowo-styrenowych. Najbardziej znanym i rozpowszechnionym kopolimerem jest tworzywo ABS, uzyskiwany w polimeryzacji akrylonitrylu, butadienu oraz styrenu. Styren jest współcześnie jednym z podstawowych surowców dla przemysłu tworzyw sztucznych.
Styren używany jest w licznych syntezach organicznych. W większości zużywany do produkcji polistyrenu, kopolimerów, gumy syntetycznej. Jest rozpuszczalnikiem i składnikiem żywic poliestrowych.
Zagrożenia
Styren do organizmu człowieka dostaje się poprzez układ oddechowy, a także (w niewielkim stopniu) przez skórę. Substancja ta jest pochłaniana podczas bezpośredniej inhalacji w 60–80% i osadza się głównie w tkance tłuszczowej. Styren działa przede wszystkim depresyjnie na ośrodkowy układ nerwowy i obwodowy, przez interkalację nieprzereagowanego styrenu do neurylemmy i zaburzanie przewodnictwa nerwowego, jak i na poprzez oddziaływanie różnych form tlenku styrenu na poszczególne elementy tego układu. W organizmie człowieka działa depresyjnie na ośrodkowy układ nerwowy oraz drażniąco na błony śluzowe. Może prowadzić do marskości wątroby. W organizmie człowieka styren jest metabolizowany w wątrobie, głównie szlakiem prowadzącym przez tlenek styrenu, glikol styrenowy, kwas migdałowy lub kwas benzoesowy do kwasów hipurowego i fenyloglioksylowego, które są wydalane z moczem.
Amerykański Rejestr Substancji Toksycznych i Schorzeń (Agency for Toxic Substances and Disease Registry – ATSDR) stwierdza, że wystawienie organizmu człowieka na działanie styrenu w dużym stężeniu (stężenie styrenu 1000 razy większe niż w normalnym środowisku) może działać na układ nerwowy. Skutkami są zmniejszenie szybkość przewodności nerwowej i obniżenie czasu reakcji. U osób narażonych na kontakt ze styrenem mogą, wystąpić objawy zatrucia ostrego lub przewlekłego, w zależności od dawki, czasu i częstotliwości ekspozycji. Opary styrenu w małych stężeniach mogą wywołać łzawienie oczu i metaliczny smak w ustach, w stężeniach ok. 800 mg/m³ – ból i zaczerwienienie spojówek, a w większych – kaszel, zawroty głowy, zaburzenia równowagi, osłabienie, bóle głowy, zmęczenie, nerwowość, a także porażenie górnych dróg oddechowych i zaburzenia widzenia. Przerwanie ekspozycji na ten związek powoduje cofnięcie objawów. Kontynuowanie narażenia wywołuje senność, zaburzenia świadomości, może także wystąpić porażenie ośrodka oddechowego i śmierć. Skażenie skóry ciekłym styrenem może wywołać jej ból i zaczerwienienie. Skażenie oczu ciekłym styrenem wywołuje ból i zaczerwienienie spojówek. Po spożyciu, związek ten wywołuje ból gardła, ból brzucha, nudności, wymioty i ogólne objawy zatrucia drogą pokarmową. W przypadku zatrucia przewlekłego, objawami są przewlekłe zapalenie skóry, przewlekłe zapalenie spojówek, upośledzenie węchu, zaburzenia funkcji psychicznych, spowolnienie reakcji, zmiany w zapisie elektroencefalograficznym. Styren został sklasyfikowany przez Międzynarodowa Agencje Do Walki z Rakiem, jako substancja potencjalnie rakotwórcza (klasa rakotwórczości B2). Amerykański Departament Ochrony Środowiska (U.S. Environmental Protection Agency – EPA) nie klasyfikuje styrenu jako substancję rakotwórczą, lecz jako substancję podejrzewaną o działanie rakotwórcze, a także jako wykazującą działanie toksyczne na układ pokarmowy, nerki i układ oddechowy.
Styren zgodnie z rozporządzeniem Ministra Zdrowia z dnia 28 września 2005 r. w sprawie wykazu substancji niebezpiecznych wraz z ich klasyfikacją i oznakowaniem[14] jest sklasyfikowany jako substancja niebezpieczna, wykazująca m.in. działanie drażniące na oczy i skórę. Obecność ww. substancji w zabawkach narusza przepisy § 17 ust. 3 rozporządzenia Ministra Gospodarki z dnia 14 listopada 2003 roku w sprawie zasadniczych wymagań dla zabawek[15].
Przypisy
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4 .
- ↑ a b c d e f Haynes 2014 ↓, s. 3-488.
- ↑ Haynes 2014 ↓, s. 5-198.
- ↑ a b c Haynes 2014 ↓, s. 6-72.
- ↑ Haynes 2014 ↓, s. 6-234.
- ↑ Haynes 2014 ↓, s. 9-59.
- ↑ a b Styren, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2015-12-09] (ang.).
- ↑ a b c Haynes 2014 ↓, s. 16-28.
- ↑ Styren (nr W323306) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2015-12-09]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Styren (nr W323306) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2015-12-09]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b c Podręczny słownik chemiczny, RomualdR. Hassa (red.), JanuszJ. Mrzigod (red.), JanuszJ. Nowakowski (red.), Katowice: Videograf II, 2004, s. 382, ISBN 83-7183-240-0 .
- ↑ MaciejM. Iłowiecki MaciejM., Dzieje nauki polskiej, Warszawa: Interpress, 1981, s. 266, ISBN 83-223-1876-6, OCLC 830296583 .
- ↑
 Lindlar, H., Dubuis, R. Palladium Catalyst for Partial Reduction of Acetylenes. „Organic Syntheses”. 46, s. 89, 1966. DOI: 10.15227/orgsyn.046.0089.
Lindlar, H., Dubuis, R. Palladium Catalyst for Partial Reduction of Acetylenes. „Organic Syntheses”. 46, s. 89, 1966. DOI: 10.15227/orgsyn.046.0089. - ↑ Dz.U. z 2005 r. nr 201, poz. 1674.
- ↑ Dz.U. z 2003 r. nr 210, poz. 2045.
Bibliografia
- CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 95, Boca Raton: CRC Press, 2014, ISBN 978-1-4822-0867-2 (ang.).
- Britannica: science/styrene
- БРЭ: 4166735
- SNL: styren
- DSDE: styren


















