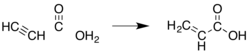
Kwas akrylowy
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C3H4O2 | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | CH | ||||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 72,06 g/mol | ||||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwna ciecz o nieprzyjemnym, gryzącym zapachu[1] | ||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 79-10-7 | ||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6581 | ||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB02579 | ||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | alkohol allilowy, kwas krotonowy, kwas cynamonowy, akroleina, akrylamid | ||||||||||||||||||||||||||||||||||||||||||
| Pochodne | akrylany (np. akrylan metylu) | ||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
Kwas akrylowy – organiczny związek chemiczny, najprostszy nienasycony kwas karboksylowy. Jego sole i estry to akrylany.
Otrzymywanie
Współcześnie otrzymywany jest głównie przez utlenianie propylenu. W zależności od warunków utlenianie przebiega jednoetapowo[8]:
- 2CH
2=CH−CH
3 + 3O
2 → 2CH
2=CH−COOH + 2H
2O
lub dwuetapowo[8]:
- 2CH
2=CH−CH
3 + 2O
2 → 2CH
2=CH−CHO + 2H
2O - 2CH
2=CH−CHO + O
2 → 2CH
2=CH−COOH
Badane są też możliwości jego produkcji z tańszego propanu[9].
Dawniej stosowano szereg innych metod, np.[8]:
- z acetylenu:
- niskotemperaturowy (40 °C) proces opracowany przez Waltera Reppego:
- 4C
2H
2 + 4H
2O + 2HCl + Ni(CO)
4 → 4CH
2=CH−COOH + H
2↑ + NiCl
2
- wersja wysokotemperaturowa (200 °C, 140 atm, w obecności katalizatora NiBr
2 − CuBr
2):
- hydroliza akrylonitrylu CH
2=CH
2−C≡N - piroliza kwasu octowego do ketenu
- CH
3COOH → CH
2=C=O + H
2O - Keten w reakcji z formaldehydem daje β-propiolakton:
- CH
2=C=O + CH
2=O →
- Związek ten za pomocą hydrolizy kwasowej przeprowadza się w kwas akrylowy
- HCN +
 → HO−CH
→ HO−CH
2CH
2−CN - Powstałą cyjanohydrynę etylenu hydrolizuje się w warunkach kwasowych do hydroksykwasu a następnie poddaje się dehydratacji (eleminacji -OH) otrzymując rzeczony kwas.
- HO-CH2-CH2-CN + H2O -> NH3 + HO-CH2-CH2-COOH -> CH2=CH−COOH + H2O
Metody te są stopniowo wycofywane z użycia[8].
Właściwości chemiczne
Kwas akrylowy ulega reakcjom typowym dla alifatycznych kwasów karboksylowych, jak i związków nienasyconych. Jego reaktywność jest podwyższona z powodu występowania układu wiązań sprzężonych C=C−C=O. Atom węgla β ma silny charakter elektrofilowy, dzięki czemu kwas akrylowy łatwo ulega reakcji addycji nukleofilowej. Bardzo łatwo ulega polimeryzacji, która jest silnie egzotermiczna i ma gwałtowny przebieg[8].
Przypisy
- ↑ a b c d e f g h i j Acrylic acid, [w:] GESTIS-Stoffdatenbank, Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung, ZVG: 014360 [dostęp 2017-10-18] (niem. • ang.).
- ↑ a b Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4 .
- ↑ a b c d e f Haynes 2016 ↓, s. 3-8.
- ↑ Haynes 2016 ↓, s. 5-88.
- ↑ Haynes 2016 ↓, s. 15-13.
- ↑ Kwas akrylowy, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2017-10-18] (ang.).
- ↑ a b Kwas akrylowy (nr 147230) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2017-10-18]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b c d e Acrylic Acid andA.A. Derivatives Acrylic Acid andA.A., Takashi Ohara, Takahisa Sato, Noboru Shimizu, Günter Prescher Helmut Schwind, Otto Weiberg, Klaus Marten, Helmut Greim, [w:] Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley‐VCH, 2005, DOI: 10.1002/14356007.a01_161.pub2 (ang.).
- ↑ MichaelM. Hävecker MichaelM. i inni, Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid, „Journal of Catalysis”, 285 (1), 2012, s. 48–60, DOI: 10.1016/j.jcat.2011.09.012 (ang.).
Bibliografia
- CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, ISBN 978-1-4987-5429-3 (ang.).
- Britannica: science/acrylic-acid
- SNL: akrylsyre
- Catalana: 0155548
- DSDE: akrylsyre