Butanol
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C4H10O | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | C | |||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 74,12 g/mol | |||||||||||||||||||||||||||||||||||||||||
| Wygląd | przezroczysta, bezbarwna ciecz[1] | |||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 71-36-3 | |||||||||||||||||||||||||||||||||||||||||
| PubChem | 263 | |||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB02145 | |||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
Butanol, alkohol butylowy, C
4H
9OH – organiczny związek chemiczny z grupy alkoholi. Jest używany głównie jako rozpuszczalnik oraz produkt przejściowy w reakcjach chemicznych, rozważa się jego stosowanie jako paliwa.
Izomery
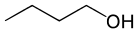
Butanol może występować w czterech formach izomerycznych. Nazwa „butanol” (lub „alkohol butylowy”) nie jest jednoznaczna, odnosi się jednak zazwyczaj do n-butanolu (1-butanolu), czyli związku, w którym grupa hydroksylowa przyłączona jest do skrajnego atomu węgla prostego łańcucha czterowęglowego: CH3CH2CH2CH2OH. Ten sam łańcuch połączony z grupą hydroksylową przez wiązanie z jednym z wewnętrznych atomów węgla nosi nazwę sec-butanol (2-butanol) i występuje w postaci dwóch enancjomerów. Izomer o rozgałęzionym szkielecie węglowym z grupą hydroksylową powiązaną z zewnętrznym atomem węgla to izobutanol (2-metylo-1-propanol), natomiast rozgałęziony izomer z grupą hydroksylową powiązaną z wewnętrznym atomem węgla to tert-butanol (t-butanol, 2-metylo-2-propanol).
 |  |  |  |  |
 |  |  |  |  |
| n-butanol butan-1-ol | (R)-sec-butanol (R)-butan-2-ol | (S)-sec-butanol (S)-butan-2-ol | izobutanol 2-metylopropan-1-ol | tert-butanol 2-metylopropan-2-ol |
n-Butanol jest gorzej rozpuszczalny w wodzie niż etanol i lepiej niż cięższe alkohole (o większej ilości atomów węgla). Jest tak, ponieważ alkohole zawierają z jednej strony polarną grupę hydroksylową, zwiększającą rozpuszczalność w wodzie, z drugiej hydrofobowy łańcuch alkilowy, który tę rozpuszczalność pogarsza. Metanol, etanol i propanol są dobrze rozpuszczalne w wodzie, gdyż przeważa tam wpływ struktury polarnej, natomiast butanol jest słabo rozpuszczalny, gdyż oba czynniki są w równowadze. Podobnie jak większość alkoholi, butanol jest szkodliwy.
Izomery butanolu mają mocno zróżnicowane temperatury krzepnięcia i wrzenia. Także ich rozpuszczalności w wodzie są różne – rosną wraz z rzędowością.
Zastosowania
Butanol jest stosowany jako rozpuszczalnik w procesach chemicznych oraz przemyśle włókienniczym. Pełni także rolę produktu pośredniego w reakcjach chemicznych. Jest również używany jako rozpuszczalnik do farb, składnik lakierów, olejów hydraulicznych oraz płynów hamulcowych. Na bazie butanolu produkowane są niektóre perfumy. Sole butanolu (butanolany) używane są jako produkt pośredni w reakcjach chemicznych.
Zdolność n-butanolu do rozpuszczania pewnej ilości wody wykorzystywana jest do zatężania wodnych roztworów kwasów nukleinowych[13] oraz do ich oczyszczania przez wytrącanie[14].
Butanol jako paliwo
Butanol może być wykorzystany jako paliwo dla silników wewnętrznego spalania. Ponieważ jego właściwości zbliżone są do benzyny (patrz tabela), butanol może być użyty w 100% jako zamiennik benzyny bez konieczności modyfikacji silnika[15].
Porównanie z innymi paliwami:
| Paliwo | Wartość energetyczna | Ciepło parowania | RON | MON |
|---|---|---|---|---|
| Benzyna | 32 MJ/l | 0,36 MJ/kg | 91–99 | 81–89 |
| Butanol | 29,2 MJ/l | 0,43 MJ/kg | 96 | 78 |
| Etanol | 19,6 MJ/l | 0,92 MJ/kg | 130 | 96 |
| Metanol | 16 MJ/l | 1,2 MJ/kg | 136 | 104 |
Produkcja
Od lat 50. butanol produkowany jest przede wszystkim z paliw kopalnych. Może być produkowany także w drodze fermentacji z biomasy roślinnej (do lat 50. była to główna metoda produkcji butanolu), zazwyczaj słomy, ale również dowolnych innych odpadów roślinnych zawierających węglowodany. Proces ten odbywa się z udziałem bakterii Clostridium acetobutylicum i pozwala na uzyskiwanie butanolu o stężeniu do 7%. W ciągu ostatnich kilkudziesięciu lat odkryto także inne bakterie zdolne do wydajnej produkcji butanolu (np. C. beijerinckii, C. aurantibutyricum i C. butylicum[16]). Prowadzone są badania nad uzyskaniem szczepów produkujących butanol w większym stężeniu (ponad 9%), umożliwiającym samoczynne rozdzielanie się butanolu od fazy wodnej w trakcie fermentacji[17]. Butanol uzyskany na drodze fermentacji biomasy nazywany jest biobutanolem, a ustawa o biopaliwach nie ogranicza jego rozproszonej produkcji.
Rozważana jest także produkcja butanolu z etanolu przez elektrolizę:
- 4C2H5OH → 2C4H9OH + 2H2 + O2
Przypisy
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4 .
- ↑ a b c d e Haynes 2016 ↓, s. 3-78.
- ↑ Haynes 2016 ↓, s. 5-173.
- ↑ a b c d Haynes 2016 ↓, s. 5-142.
- ↑ a b c Haynes 2016 ↓, s. 6-68.
- ↑ Haynes 2016 ↓, s. 6-243.
- ↑ Haynes 2016 ↓, s. 6-190.
- ↑ Haynes 2016 ↓, s. 9-60.
- ↑ butan-1-ol, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2016-12-27] (ang.).
- ↑ a b Haynes 2016 ↓, s. 16-18.
- ↑ a b c d 1-Butanol (nr 281549) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2016-12-27]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ 1-Butanol (nr 281549) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2016-12-27]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ G. Cathala, C. Brunel. Use of n-butanol for efficient recovery of minute amounts of small RNA fragments and branched nucleotides from dilute solutions. „Nucleic Acids Res”. 18 (1), s. 201, 1990. DOI: 10.1093/nar/18.1.201. PMID: 1689817. PMCID: PMC330238.
- ↑ M. Sawadogo, M.W. Van Dyke. A rapid method for the purification of deprotected oligodeoxynucleotides. „Nucleic Acids Res”. 19 (3), s. 674, 1991. DOI: 10.1093/nar/19.3.674. PMID: 2011537. PMCID: PMC333665.
- ↑ ButylFuel.
- ↑ H.A. George, J.L. Johnson, W.E. Moore, L.V. Holdeman i inni. Acetone, Isopropanol, and Butanol Production by Clostridium beijerinckii (syn. Clostridium butylicum) and Clostridium aurantibutyricum.. „Appl Environ Microbiol”. 45 (3), s. 1160–1163, 1983. PMID: 16346237. PMCID: PMC242427.
- ↑ Pierrot, P., Fick, M., Engasser, J.M. Continuous acetone-butanol fermentation with high productivity by cell ultrafiltration and recycling. „Biotechnol Lett”. 8 (4), s. 253–256, 1986. DOI: 10.1007/BF01030507.
Bibliografia
- CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, ISBN 978-1-4987-5429-3 (ang.).
- p
- d
- e
|
- Britannica: science/n-butyl-alcohol
















