Trifluorättiksyra
| Trifluorättiksyra | |
  | |
| Systematiskt namn | Trifluoretansyra |
|---|---|
| Övriga namn | TFA |
| Kemisk formel | C2HF3O2 eller CF3COOH |
| Molmassa | 114,0233 g/mol |
| Utseende | Färglös vätska |
| CAS-nummer | 76-05-1 |
| SMILES | FC(F)(F)C(O)=O |
| Egenskaper | |
| Densitet | 1,48 g/cm³ |
| Löslighet (vatten) | Blandbar |
| Smältpunkt | -15 °C |
| Kokpunkt | 72 °C |
| Faror | |
| Huvudfara |  Frätande Frätande |
| NFPA 704 |
0 3 0 |
| LD50 | 200 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
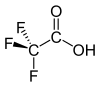
Trifluorättiksyra (TFA) är en fluorerad karboxylsyra med kemisk formel CF3COOH. Ämnets salter och estrar kallas trifluoracetater eller trifluoretanoater.
Egenskaper
TFA är en stark syra (pKa = 0,3) på grund av fluoratomernas starka elektronegativa inverkan.
Framställning
Trifluorättiksyra framställs industriellt genom elektrosyntes av acetylklorid (CH3COCl) eller ättiksyraanhydrid ((CH3CO)2O) med vätefluorid (HF), vilket ger trifluoracetylfluorid (CF3COF) som sedan hydrolyseras i vatten och ger trifluorättiksyra.
- 1.
- 2.
Användning
TFA används som reaktant inom organisk syntes. Den används bland annat för att framställa trifluorättiksyraanhydrid ((CF3CO)2O) och 2,2,2-trifluoroetanol (C2F3H2OH).
Trifluorättiksyra används också som referensmaterial för kalibrering vid NMR-spektroskopi.
Se även
Källor
- Material Safety Data Sheet Mallinckrodt Baker
- Säkerhetsdatablad[död länk] Fisher Scientific AB
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Trifluoroacetic acid, tidigare version.











