Jod-pentoksid
| Jod pentoksid | |||
|---|---|---|---|
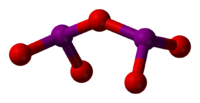 | |||
 | |||
| IUPAC ime |
| ||
| Drugi nazivi | jod(V) oksid; anhidrid jodne kiseline | ||
| Identifikacija | |||
| CAS registarski broj | 12029-98-0  Y Y | ||
| PubChem[1][2] | 159402 | ||
| ChemSpider[3] | 140179  Y Y | ||
| MeSH | Iodine+pentoxide | ||
| ChEBI | 29914 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | I2O5 | ||
| Molarna masa | 333.81 g/mol | ||
| Agregatno stanje | bela kristalna supstanca[4] | ||
| Gustina | 4.980 g cm−3[4] | ||
| Tačka topljenja | ? °C | ||
| Tačka ključanja | ? °C | ||
| Opasnost | |||
| Opasnost u toku rada | oksidant | ||
|
| |||
| Infobox references | |||
Jod-pentoksid je oksid joda hemijske formule I2O5, gde je oksidacioni broj joda +5.
Dobijanje
Može se dobiti zagrevanjem jodne kiseline na temperaturi od oko 170 °C, jer se ona tada raspada uz gubitak vode[5]:
Svojstva
Jod-pentoksid je bela kristalna supstanca, za koju važi da je postojanija nego bilo koji drugi oksid hlora ili broma. Ipak, iznad 200 °C se raspada na jod i kiseonik. Sa vodom gradi jodnu kiselinu, te se smatra njenim anhidridom.[5]
| Osobina | Vrednost |
|---|---|
| Particioni koeficijent[6] (ALogP) | 1,3 |
| Rastvorljivost[7] (logS, log(mol/L)) | 4,1 |
| Polarna površina[8] (PSA, Å2) | 77,5 |
Primena
Ovaj oksid je jako oksidaciono sredstvo, pa može da oksiduje ugljen-monoksid, što je važno u otkrivanju ovog gasa u smeši, čak i u malim količinama:
Reagens koji se koristi u ovu svrhu i koji sadrži jod-pentoksid se naziva hulmanit.[5]
Reference
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519. edit
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846. edit
- ↑ 4,0 4,1 Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (2nd ed.), Oxford: Butterworth-Heinemann, pp. 851-852. ISBN 978-0-7506-3365-9.
- ↑ 5,0 5,1 5,2 Parkes, G. D. & Fil, D. 1973. Melorova moderna neorganska hemija. Naučna knjiga. Beograd.
- ↑ Ghose, A.K., Viswanadhan V.N., and Wendoloski, J.J. (1998). „Prediction of Hydrophobic (Lipophilic) Properties of Small Organic Molecules Using Fragment Methods: An Analysis of AlogP and CLogP Methods”. J. Phys. Chem. A 102: 3762-3772. DOI:10.1021/jp980230o.
- ↑ Tetko IV, Tanchuk VY, Kasheva TN, Villa AE. (2001). „Estimation of Aqueous Solubility of Chemical Compounds Using E-State Indices”. Chem Inf. Comput. Sci. 41: 1488-1493. DOI:10.1021/ci000392t. PMID 11749573.
- ↑ Ertl P., Rohde B., Selzer P. (2000). „Fast calculation of molecular polar surface area as a sum of fragment based contributions and its application to the prediction of drug transport properties”. J. Med. Chem. 43: 3714-3717. DOI:10.1021/jm000942e. PMID 11020286.
Literatura
Spoljašnje veze
 | Portal Hemija |

- Iodine pentoxide
p • r • u Jodidi | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| HI | He | ||||||||||||||||||||||||||||||
| LiI | BeI2 | BI3 | CI4 | NI3 | I2O4, I2O5, I4O9 | IF, IF3, IF5, IF7 | Ne | ||||||||||||||||||||||||
| NaI | MgI2 | AlI3 | SiI4 | PI3, P2I4 | S | ICl, ICl3 | Ar | ||||||||||||||||||||||||
| KI | CaI2 | Sc | TiI4 | VI3 | Cr | MnI2 | Fe | CoI2 | NiI2 | CuI | ZnI2 | Ga2I6 | GeI2, GeI4 | AsI3 | Se | IBr | Kr | ||||||||||||||
| RbI | SrI2 | Y | ZrI4 | Nb | Mo | Tc | Ru | Rh | Pd | AgI | CdI2 | InI3 | SnI4, SnI2 | SbI3 | TeI4 | I | Xe | ||||||||||||||
| CsI | BaI2 | Hf | Ta | W | Re | Os | Ir | Pt | AuI | Hg2I2, HgI2 | TlI | PbI2 | BiI3 | Po | At | Rn | |||||||||||||||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Uuq | Uup | Uuh | Uus | Uuo | |||||||||||||||
| ↓ | |||||||||||||||||||||||||||||||
| La | Ce | Pr | Nd | Pm | SmI2 | Eu | Gd | TbI3 | Dy | Ho | Er | Tm | Yb | Lu | |||||||||||||||||
| Ac | ThI4 | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||||||||||||||||







