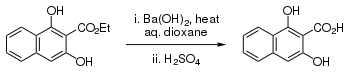Wodorotlenek baru
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | Ba(OH)2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa | 171,34 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | białe ciało stałe | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 17194-00-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 28387 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inne aniony | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inne kationy | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Wodorotlenek baru Ba(OH)2 – nieorganiczny związek chemiczny. Roztwór wodorotlenku baru jest silną zasadą, w stanie stałym występuje w postaci białych granulek lub proszku.
Otrzymywanie
Wodorotlenek baru otrzymywany jest w wyniku reakcji tlenku baru (BaO) z wodą. Krystalizuje jako ośmiowodny hydrat (Ba(OH)2·8H2O), który może zostać odwodniony do związku jednowodnego (monohydratu) poprzez ogrzewanie na powietrzu lub odwodniony całkowicie podczas ogrzewania w 100 °C pod próżnią.
Zastosowanie
Wodorotlenek baru jest używany w chemii analitycznej do miareczkowania słabych kwasów, zwykle kwasów organicznych. Jest „czystym odczynnikiem” wolnym od zanieczyszczeń wodorotlenku sodu i wodorotlenku potasu. Rozpuszczony nie zawiera niepożądanych węglanów (węglan baru jest nierozpuszczalny w wodzie). Używany do miareczkowania z takimi wskaźnikami jak fenoloftaleina lub tymoloftaleina zmieniających kolor w środowisku alkalicznym, bez ryzyka błędu miareczkowania spowodowanego słabymi jonami węglanowymi. Wodny nasycony roztwór wodorotlenku baru nazywany jest wodą barytową.
Wodorotlenek baru używany jest w syntezie organicznej jako silna zasada, np.
- do syntezy cyklopentanonu[4]:
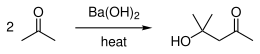
- do syntezy alkoholu diacetonowego[5]:
oraz w innych reakcjach.
Inne zastosowania
- do neutralizacji rozlanych kwasów
- składnik preparatów homeopatycznych
Zagrożenia
Wodorotlenek baru jest żrący i szkodliwy dla zdrowia.
Przypisy
- ↑ a b c Wodorotlenek baru (nr 433373) w katalogu produktów Sigma-Aldrich (Merck). [dostęp 2011-01-16].
- ↑
 Karl Meyer, Henry S. Bloch. Naphthoresorcinol. „Org. Synth.”. 25, s. 73, 1945. DOI: 10.15227/orgsyn.025.0073.
Karl Meyer, Henry S. Bloch. Naphthoresorcinol. „Org. Synth.”. 25, s. 73, 1945. DOI: 10.15227/orgsyn.025.0073. - ↑
 George Bosworth Brown. Methylsuccinic acid. „Org. Synth.”. 26, s. 45, 1946. DOI: 10.15227/orgsyn.026.0054.
George Bosworth Brown. Methylsuccinic acid. „Org. Synth.”. 26, s. 45, 1946. DOI: 10.15227/orgsyn.026.0054. - ↑
 J. F. Thorpe, G. A. R. Kon. Cyclopentanone. „Org. Synth.”. 5, s. 37, 1925. DOI: 10.15227/orgsyn.005.0037.
J. F. Thorpe, G. A. R. Kon. Cyclopentanone. „Org. Synth.”. 5, s. 37, 1925. DOI: 10.15227/orgsyn.005.0037. - ↑
 J. B. Conant, Niel Tuttle. Diacetone alcohol. „Org. Synth.”. 1, s. 45, 1921. DOI: 10.15227/orgsyn.001.0045.
J. B. Conant, Niel Tuttle. Diacetone alcohol. „Org. Synth.”. 1, s. 45, 1921. DOI: 10.15227/orgsyn.001.0045.