| NR1D1 |
|---|
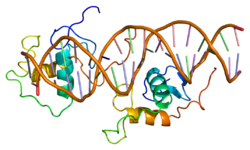 |
|
| Structures disponibles |
|---|
| PDB | Recherche d'orthologue: PDBe RCSB |
|---|
| Identifiants PDB |
|---|
1A6Y, 1GA5, 1HLZ, 3N00 |
|
|
| Identifiants |
|---|
| Aliases | NR1D1 |
|---|
| IDs externes | OMIM: 602408 MGI: 2444210 HomoloGene: 23324 GeneCards: NR1D1 |
|---|
| Position du gène (Homme) |
|---|
 | | Chr. | Chromosome 17 humain[1] |
|---|
| | Locus | 17q21.1 | Début | 40,092,793 bp[1] |
|---|
| Fin | 40,100,589 bp[1] |
|---|
|
| Position du gène (Souris) |
|---|
 | | Chr. | Chromosome 11 (souris)[2] |
|---|
| | Locus | 11|11 D | Début | 98,658,758 bp[2] |
|---|
| Fin | 98,666,159 bp[2] |
|---|
|
| Expression génétique |
|---|
| Bgee | | Humain | Souris (orthologue) |
|---|
| Fortement exprimé dans | - skin of leg
- skin of abdomen
- pancreatic ductal cell
- poumon droit
- ectocervix
- muscle tibial antérieur
- paraflocculus of cerebellum
- Brodmann area 10
- right hemisphere of cerebellum
- mamelon
|
| | Fortement exprimé dans | - neural layer of retina
- lèvre
- cheville
- gyrus frontal supérieur
- œsophage
- valve aortique
- dentate gyrus of hippocampal formation granule cell
- primary visual cortex
- muscle triceps brachial
- articulation talo-crurale
|
| | Plus de données d'expression de référence |
|
|---|
| BioGPS | 
 | | Plus de données d'expression de référence |
|
|---|
|
| Gene Ontology |
|---|
| Fonction moléculaire | - liaison ADN
- sequence-specific DNA binding
- RNA polymerase II transcription regulatory region sequence-specific DNA binding
- transcription corepressor activity
- DNA-binding transcription factor activity
- zinc ion binding
- liaison ion métal
- RNA polymerase II cis-regulatory region sequence-specific DNA binding
- steroid hormone receptor activity
- DNA-binding transcription repressor activity, RNA polymerase II-specific
- nuclear receptor activity
- core promoter sequence-specific DNA binding
- liaison protéique
- heme binding
- transcription corepressor binding
- DNA-binding transcription factor activity, RNA polymerase II-specific
- E-box binding
- transcription cis-regulatory region binding
- transcription factor binding
- nuclear receptor coactivator activity
- signaling receptor activity
| | Composant cellulaire | - cytoplasme
- prolongement cellulaire
- épine dendritique
- nucléoplasme
- dendrite
- noyau
- corps nucléaire
- RNA polymerase II transcription regulator complex
| | Processus biologique | - différenciation cellulaire
- regulation of insulin secretion involved in cellular response to glucose stimulus
- regulation of transcription, DNA-templated
- processus rythmique
- circadian temperature homeostasis
- positive regulation of bile acid biosynthetic process
- negative regulation of transcription by RNA polymerase II
- circadian regulation of gene expression
- regulation of fat cell differentiation
- transcription, DNA-templated
- régulation positive de la transcription dépendante de l'ADN
- regulation of lipid metabolic process
- glycogen biosynthetic process
- regulation of circadian rhythm
- rythme circadien
- proteasomal protein catabolic process
- transcription initiation from RNA polymerase II promoter
- response to leptin
- negative regulation of transcription, DNA-templated
- cellular response to lipopolysaccharide
- regulation of type B pancreatic cell proliferation
- negative regulation of toll-like receptor 4 signaling pathway
- steroid hormone mediated signaling pathway
- intracellular receptor signaling pathway
- cholesterol homeostasis
- développent d'un organisme multicellulaire
- hormone-mediated signaling pathway
- response to lipid
- positive regulation of transcription by RNA polymerase II
- negative regulation of cold-induced thermogenesis
- protein destabilization
- regulation of circadian sleep/wake cycle
- negative regulation of I-kappaB kinase/NF-kappaB signaling
- negative regulation of inflammatory response
- negative regulation of astrocyte activation
- cellular response to interleukin-1
- cellular response to tumor necrosis factor
- negative regulation of neuroinflammatory response
- negative regulation of microglial cell activation
| | Sources:Amigo / QuickGO |
|
| Orthologues |
|---|
| Espèces | Homme | Souris |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (mRNA) | | |
|---|
| RefSeq (protéine) | | |
|---|
| Localisation (UCSC) | Chr 17: 40.09 – 40.1 Mb | Chr 11: 98.66 – 98.67 Mb |
|---|
| Publication PubMed | [3] | [4] |
|---|
|
| Wikidata |
| Voir/Editer Humain | Voir/Editer Souris |
|
Le NR1D1 (NR sous-famille 1 groupe D membre1), aussi appelé Rev-erbα, est un récepteur nucléaire dont le gène est NR1D1 situé sur le chromosome 17 humain.
Rôles
Il joue un rôle dans le rythme circadien, avec une activité qui augmente le matin[5]. Son expression dans les thrombocytes favorise l'activation de ces derniers et la formation de thrombus[6]. Il influence le métabolisme hépatique[7].
Il régule le stress oxydatif, l'inflammation et stabilise la plaque d'athérome[8].
Il inhibe l'acotinase 2 mitochondrial. L'inactivation du NR1D1 conduit à augmenter l'activité de l'acotinase 2 et pourrait être bénéfique dans l'évolution d'un anévrisme de l'aorte abdominale[9].
Notes et références
- ↑ a b et c GRCh38: Ensembl release 89: ENSG00000126368 - Ensembl, May 2017
- ↑ a b et c GRCm38: Ensembl release 89: ENSMUSG00000020889 - Ensembl, May 2017
- ↑ « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ Montaigne D, Marechal X, Modine T et al. Daytime variation of perioperative myocardial injury in cardiac surgery and its prevention by Rev-erbα antagonism: a single-centre propensity-matched cohort study and a randomised study, Lancet, 2018;391:59–69
- ↑ Shi J, Tong R, Zhou M et al. Circadian nuclear receptor Rev-erbα is expressed by platelets and potentiates platelet activation and thrombus formation, Eur Heart J, 2022;43:2317–2334
- ↑ Hunter AL, Pelekanou CE, Adamson A et al. Nuclear receptor REVERBα is a state-dependent regulator of liver energy metabolism, Proc Natl Acad Sci USA, 2020; 117:25869–25879
- ↑ Wu Z, Liao F, Luo G et al. NR1D1 deletion induces rupture-prone vulnerable plaques by regulating macrophage pyroptosis via the NF-κB/NLRP3 inflammasome pathway, Oxid Med Cell Longev, 2021;2021:5217572
- ↑ Sun LY, Lyu YY, Zhang HY et al. Nuclear receptor NR1D1 regulates abdominal aortic aneurysm development by targeting the mitochondrial tricarboxylic acid cycle enzyme aconitase-2, Circulation, 2022;146:1591-1609
 Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire

 Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire 















