| LCAT |
|---|
 |
|
| Structures disponibles |
|---|
| PDB | Recherche d'orthologue: PDBe RCSB |
|---|
| Identifiants PDB |
|---|
4X96, 4XWG, 4XX1, 5BV7 |
|
|
| Identifiants |
|---|
| Aliases | LCAT |
|---|
| IDs externes | OMIM: 606967 MGI: 96755 HomoloGene: 68042 GeneCards: LCAT |
|---|
| Position du gène (Homme) |
|---|
 | | Chr. | Chromosome 16 humain[1] |
|---|
| | Locus | 16q22.1 | Début | 67,939,750 bp[1] |
|---|
| Fin | 67,944,131 bp[1] |
|---|
|
| Position du gène (Souris) |
|---|
 | | Chr. | Chromosome 8 (souris)[2] |
|---|
| | Locus | 8 D3|8 53.06 cM | Début | 106,666,183 bp[2] |
|---|
| Fin | 106,670,014 bp[2] |
|---|
|
| Expression génétique |
|---|
| Bgee | | Humain | Souris (orthologue) |
|---|
| Fortement exprimé dans | - right lobe of liver
- right hemisphere of cerebellum
- nerf tibial
- left lobe of thyroid gland
- apex of heart
- right lobe of thyroid gland
- aorte ascendante
- artère coronaire droite
- endocol
- body of uterus
|
| | Fortement exprimé dans | - left lobe of liver
- lumbar subsegment of spinal cord
- dentate gyrus of hippocampal formation granule cell
- cerebellar cortex
- Vésicule vitelline
- primary visual cortex
- CA3 field
- nerf optique
- hippocampus proper
- gyrus frontal supérieur
|
| | Plus de données d'expression de référence |
|
|---|
| BioGPS | |
|---|
|
| Gene Ontology |
|---|
| Fonction moléculaire | - activité de transférase
- O-acyltransferase activity
- apolipoprotein A-I binding
- liaison protéique
- acyltransferase activity
- phosphatidylcholine-sterol O-acyltransferase activity
| | Composant cellulaire | - région extracellulaire
- high-density lipoprotein particle
- exosome
- milieu extracellulaire
| | Processus biologique | - processus métabolique stéroidique
- regulation of high-density lipoprotein particle assembly
- processus métabolique lipidique
- cholesterol transport
- cholesterol metabolic process
- cholesterol esterification
- very-low-density lipoprotein particle remodeling
- phospholipid metabolic process
- lipoprotein biosynthetic process
- cholesterol homeostasis
- phosphatidylcholine biosynthetic process
- phosphatidylcholine metabolic process
- reverse cholesterol transport
- high-density lipoprotein particle remodeling
| | Sources:Amigo / QuickGO |
|
| Orthologues |
|---|
| Espèces | Homme | Souris |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (mRNA) | | |
|---|
| RefSeq (protéine) | | |
|---|
| Localisation (UCSC) | Chr 16: 67.94 – 67.94 Mb | Chr 8: 106.67 – 106.67 Mb |
|---|
| Publication PubMed | [3] | [4] |
|---|
|
| Wikidata |
| Voir/Editer Humain | Voir/Editer Souris |
|
La lécithine-cholestérol acyltransférase (LCAT) est une enzyme de type acyltransférase. Elle permet le transfert d'un acide gras à partir de la lécithine (phosphatidylcholine) sur le cholestérol dans le cadre de la formation des stérides. Son gène est LCAT situé sur le chromosome 16 humain.
Rôle
Synthétisée dans le foie, elle se localise sur les HDL notamment les pré-bêta HDL et ne peut fonctionner qu'en présence d'un cofacteur qui est l'ApoA1.
Elle va utiliser les phospholipides pour estérifier le cholestérol libre afin de donner une lipophospholipide (LPL), il s'agit d'une transestérification plasmatique du cholestérol.
C'est ainsi grâce à ce processus que le pré-bêta HDL discoïdale se transforme en HDL3 sphérique qui donnera à son tour un HDL2. On a donc la création d'un véritable "gradient" de cholestérol libre entre la cellule et l'accepteur.
 | + | 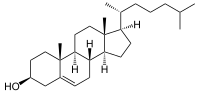 |  |  | + |  |
| Lécithine | | Cholestérol | | Lysolécithine | | Ester de cholestérol (stéride) |
| Lécithine-cholestérol acyltransférase – EC 2.3.1.43 |
En médecine
Il existe plusieurs mutations du gène LCAT entraînant une inactivation plus ou moins complète de l'enzyme[5], avec un taux sanguin abaissé en HDL-cholestérol, et des tableaux plus ou moins sévères, souvent caractérisés par un athérome précoce[6] mais pas toujours[7].
Notes et références
- ↑ a b et c GRCh38: Ensembl release 89: ENSG00000213398 - Ensembl, May 2017
- ↑ a b et c GRCm38: Ensembl release 89: ENSMUSG00000035237 - Ensembl, May 2017
- ↑ « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ Kuivenhoven JA, Pritchard H, Hill J, Frohlich J, Assmann G, Kastelein J, The molecular pathology of lecithin:cholesterol acyltransferase (LCAT) deficiency syndromes, J Lipid Res, 1997;38:191–205
- ↑ Hovingh GK, Hutten BA, Holleboom AG et al. Compromised LCAT function is associated with increased atherosclerosis, Circulation, 2005;112:879–884
- ↑ Calabresi L, Baldassarre D, Castelnuovo S et al. Functional lecithin: cholesterol acyltransferase is not required for efficient atheroprotection in humans, Circulation, 2009;120:628–635
 Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire  Portail de la médecine
Portail de la médecine





 Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire  Portail de la médecine
Portail de la médecine 





















