Natriummanganat
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
  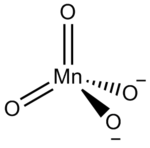 | ||||||||||
| Allgemeines | ||||||||||
| Name | Natriummanganat | |||||||||
| Andere Namen | Natriummanganat(VI) | |||||||||
| Summenformel | Na2MnO4 | |||||||||
| Kurzbeschreibung | dunkelgrüner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 164,914 g·mol−1 | |||||||||
| Aggregatzustand | fest | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Natriummanganat, Na2MnO4, ist eine chemische Verbindung des Natriums aus der Gruppe der Manganate.
Gewinnung und Darstellung
Zur Herstellung von Natriummanganat wird das Mangan(II) durch das Natriumperoxid zum entsprechenden Manganat(VI) oxidiert.[3]
Ausgehend von Mangan(IV)-oxid und von Mangan(II)-sulfat, entsteht Natriummanganat während der Oxidationsschmelze.
Eigenschaften
Mit Eisessig reagiert Natriummanganat zur Natriumpermanganat und zur Mangan(IV)-oxid.
Einzelnachweise
- ↑ Douglas M. Considine, Glenn D. Considine: Van Nostrand’s Scientific Encyclopedia. Springer Science & Business Media, 2013, ISBN 978-1-4757-6918-0, S. 2879 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Comprehensive Chemistry XI. Laxmi Publications, ISBN 81-7008-596-9, S. 868.











